차 의과학대학교 분당차병원 신경외과 한인보 교수와 미국 럿거스(Rutgers) 대학교 이기범 교수팀이 3D 하이브리드 단백질 나노스캐폴드를 개발, 퇴행성 디스크 동물모델에서 염증조절과 활성산소억제 효과에 의해 손상된 디스크를 유의하게 복원했다고 밝혔다.

이번 연구로 치료가 어려운 퇴행성 디스크로 인한 만성 요통 환자 치료에 효과적으로 활용할 수 있을 것으로 기대되고 있다.
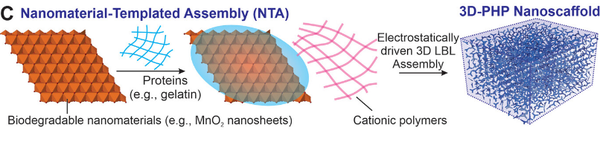
연구팀은 2D 이산화망간 나노시트를 제작해 이를 젤라틴과 결합했다. 이어 3D 하이브리드 기술을 이용해 생체 내 주입가능하고, 생분해성을 가진 3D 단백질 나노스캐폴드를 제작했다.
이어 연구팀은 쥐의 꼬리 디스크 내 수핵을 제거한 동물모델에서 약물을 포함하는 3D 하이브리드 단백질 나노스캐폴드를 주입해 손상된 디스크가 복원되는 효과를 확인했다.
특히 다발성 골수종과 백혈병에 항암효과가 있고, 염증성 질환에서 염증을 줄이는 효과가 있다고 알려진 BET(Bromodomain and Extra-terminal)억제제를 사용해 수핵 세포 특이 표지자 발현 정도와 염증반응 억제 정도, 제2형 콜라젠 생성 등을 비교했다.
그 결과 고농도(200 μg/mL) BET 억제제가 포함된 3D 하이브리드 단백질 나노스캐폴드 사용 그룹이 BET 억제제만 사용한 그룹과 저농도(100 μg/mL) 그룹 대비 2배 이상 수핵세포 표지자 발현과 염증반응 억제, 제2형 콜라젠 생성이 증가하는 것을 확인했다.
한인보 교수는 “이번 연구는 활성 산소를 효과적으로 제거하고, 항염증성 약물의 지속적인 방출을 유도할 수 있는 3D 하이브리드 단백질 나노스캐폴드를 개발함으로써 퇴행성 디스크 질환 치료를 위해 새로운 기술 플랫폼을 제공하는데 큰 의미가 있다”며 “치료가 어려운 퇴행성 디스크로 인한 만성 요통 환자 치료에 효과적으로 활용할 수 있을 것”이라고 말했다.

이번 연구결과는 국제학술지 ‘Advanced Materials(IF: 29.4)’에 게재됐다.
