한국연구재단 신흥수 교수(한양대) 연구팀이 천연 유래 성분인 탄닌산과 스트론튬 이온의 자발적 결합으로 제작된 탄닌산-스트론튬 나노입자를 활용해 대식세포의 활성을 조절함으로써 염증성 상처를 정상 피부와 유사하게 재생하는 생분해성 패치를 개발했다고 밝혔다.
보통 상처가 생기면 자연적으로 치유되지만 당뇨성 피부질환, 깊은 화상 등의 경우, 치유 과정 중 조직괴사나 흉터가 생기기 쉽다. 이때 주로 사용하는 항염증제는 장기투여 부작용은 물론 근본적 치료에는 한계가 있었다.
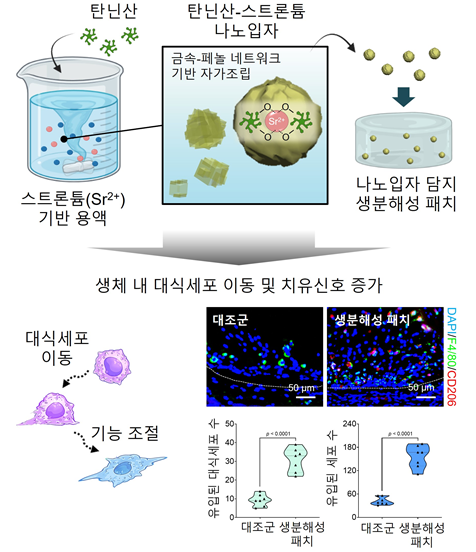
상처 치유 과정 중 초기에 유입된 이물질은 자연스럽게 대식세포에 의해 제거되는데, 대식세포는 염증반응 촉진 및 제어의 두 가지 기능을 가지고 있어 조직재생에 양날의 검으로 인식되고 있다.
최근 대식세포의 이런 기능을 조절해 염증을 제어하는 연구가 활발하지만 이를 유도하는 시스템 구축은 여전히 과제로 남아있다.
연구팀은 대식세포의 기능 조절을 통한 우리 몸의 자발적인 재생기능 촉진에 주목했다. 강력한 염증 제어 효과를 지닌 탄닌산과 세포 이동 및 조직재생 효과가 있는 스트론튬 이온을 결합해 탄닌산-스트론튬 나노입자를 제작, 하이드로젤에 담지해 생분해성 패치를 개발했다.
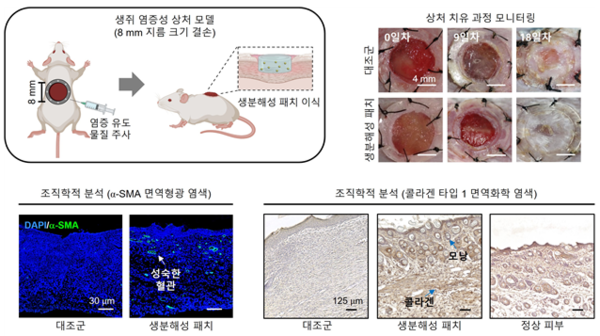
개발된 생분해성 패치를 염증성 상처에 적용했을 때, 대식세포의 상처 부위로의 유입을 촉진하며, 기능을 조절해 상처를 빠르게 치유하고 흉터가 없는 피부 재생을 유도했다. 특히 생체 내 이식 시 세포를 손상 부위로 유입시켜 재생유도 신호를 촉진함을 확인했다.
또한, 연구팀은 차세대 염기서열 분석법을 통해 탄닌산과 스트론튬이 대식세포의 기능을 조절하는 상호보완적 메커니즘을 밝혀냈다.
신흥수 교수는 “생체 내 고유한 자가 면역기능을 활용해 부작용을 최소화한 시스템으로 염증성 상처 치료를 유도한 것”이라며, “이번 기술은 다양한 하이드로젤 활용을 통해 골조직, 심장 조직 등 광범위한 조직 재생 플랫폼으로 활용할 수 있다”고 설명했다.

과학기술정보통신부와 한국연구재단이 추진하는 이공분야 기초연구사업의 지원으로 수행된 이번 연구 결과는 생체활성 물질 분야 국제학술지 ‘Bioactive Materials’에 게재됐다.
