서울대병원 이비인후과 김현직 교수 연구팀
비강 흡인 면역물질, 폐내 바이러스↓ 폐손상 회복 유전자↑

코로나 확산을 예방하고 폐렴 증상도 완화시키는 효과적인 치료제를 개발할 수 있는 길이 국내 의료진에 의해 제시됐다.
서울대병원 이비인후과 김현직 교수 연구팀이 면역물질 ‘인터페론 람다’의 바이러스 감염 제어와 면역 조절 기능을 확인하고 이 물질을 비강으로 흡입했을 때 폐내 바이러스 수치가 떨어지고 급성 폐 손상이 개선되는 것을 밝힌 것이다.
서울대병원은 김현직 교수 연구팀이 동물모델을 통해 항바이러스물질 인터페론 람다(IFN-λ)의 비강 흡입 시 코로나 감염 억제와 폐렴 증상 개선 효과가 어떠한지를 확인한 연구 결과를 18일 이같이 발표했다.
코로나 바이러스는 증상이 발현하기 전부터 감염자의 상기도에서 빠르게 증식한다. 바이러스가 사라진 후에도 호흡기에서 유발된 과면역반응으로 인해 일부 감염자에게는 지속적인 폐렴 소견이 남게 된다.
실제 연구팀의 분석에 따르면 지난해 코로나19로 입원했다가 PCR 음성을 확인받고 퇴원한 환자의 70% 이상은 X-ray에서 폐렴과 섬유화 관련 소견이 발견됐다.
이 같은 특징으로 감염 후 바이러스성 폐렴 증상을 완화하는 코로나 치료제에 대한 관심이 높은 상황이다. 또 스테로이드나 단일클론항체 치료제 등 환자의 면역반응에 따라 사용이 제한되는 기존 치료제들의 한계를 보완할 치료제가 필요한 상황이다.
연구팀은 바이러스 확산을 제어하고 폐렴 증상을 개선할 수 있는 코로나 치료제를 개발하기 위해 ‘인터페론 람다’를 활용해 호흡기 점막의 면역력을 증진시키는 흡입형 치료제 연구를 진행했다.
인터페론 람다는 바이러스 침투 시 체내에서 분비되는 항바이러스 물질이다. 특히 감염 초기 단계의 면역반응에 결정적으로 관여하는 것으로 알려졌다.
연구팀은 코로나 감염 동물 모델을 아무런 처치도 하지 않은 대조군과 감염 직후 비강 및 상기도 점막에 흡입 치료제(인터페론 람다)를 투약한 치료군으로 분류한 뒤, 두 집단의 폐 조직을 분석했다.
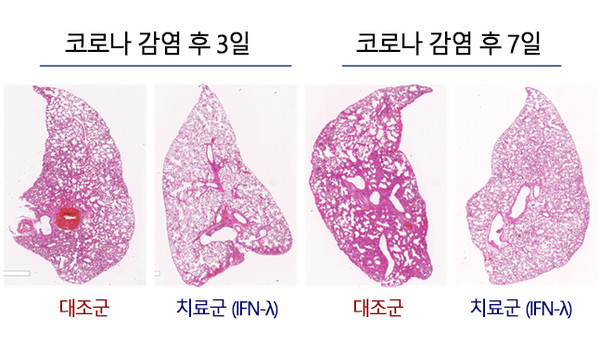
투약 3일후, 치료군의 바이러스 수치는 대조군에 비해 현저히 낮아졌다. 염증 수준을 의미하는 IL-1β, TNF-α 유전자 발현량도 치료군이 대조군보다 낮았다. 즉 인터페론 람다 비강 흡입 시 코로나가 폐까지 침투하는 것을 억제하고, 바이러스성 염증도 제거하는 효과가 있는 것이다.
인터페론 람다의 비강 흡입이 가져오는 폐렴 개선 효과를 정밀하게 확인하기 위해 폐내 유전자 발현 분석도 이뤄졌다.
그 결과, 대조군에 비해 염증 수준이 낮았던 치료군의 폐 조직에서 ▲손상 회복 ▲지질대사 ▲세포·조직재건과 관련된 유전자 발현이 우세한 것으로 확인됐다. 치료군에서 손상 회복 유전자(Fabp4)는 약 13배, 조직 재건 관련 유전자(Spp1, Saa3)은 90배 이상 더 많이 발현됐다.

이와 관련 연구팀은 인터페론 람다는 선천 면역반응을 유도해 바이러스성 급성 폐 감염을 완화시키며, 이는 인터페론 람다가 코로나 치료제의 좋은 후보 물질이 될 수 있다는 사실을 뒷받침한다고 강조했다.
한편 연구팀은 인터페론 람다의 비강 흡입이 호흡기 바이러스 감염을 제어하는 기전에 대한 추가 연구도 실시했다. 선천적으로 분비되는 인터페론 람다를 비강으로 직접 주입할 경우, 바이러스를 사멸시키고 인터페론을 유도하는 유전자 발현이 폐에서 증가하는 것으로 확인한 것이다.
인터페론 람다를 비강 흡입하면 인터페론을 유도하는 유전자를 감염 초기부터 활성화해 호흡기 감염을 효과적으로 제어할 수 있다고 연구팀은 설명했다.
김현직 교수는 “상기도 점막의 면역력을 높이는 치료제를 개발하는 과정에서 호흡기 바이러스 제어 및 폐감염 개선 물질로써 인터페론 람다의 가능성을 증명할 수 있었다”며 “현재 치료제를 실제로 개발하기 위한 후속 연구를 카이스트와 공동으로 진행 중에 있다”고 말했다.
